la démarche scientifique
activité 1 : qu’est-ce que la chimie ? qu’est-ce que la physique ?
la chimie, comme la physique sont des sciences expérimentales qui permettent de comprendre le monde autour de nous.
Cliquer ici pour plus d’informations sur ces sciences (vidéos, définitions)
activité 2 : peut-on faire confiance en nos sens ?
Nous pouvons explorer notre monde en utilisant nos sens (l’ouïe, la vue, le toucher…) mais est-ce suffisant ?
activité 3 : la démarche expérimentale
Les scientifiques utilisent une méthode pour vérifier leurs hypothèses : la démarche expérimentale.
Cliquer ici pour mieux comprendre comment les recherches et découvertes sont réalisées et vérifiées et résoudre des exercices interactifs
la sécurité en chimie
Activité 1 : Dangereux ou pas dangereux ?
La dangerosité d’une substance chimique dépend de sa nature (ce qu’il est) mais aussi de son utilisation (quantité, manière de l’utiliser…)
rappel : toute la matière est chimique mais elle peut être naturelle ou synthétique.
activité 2 : les pictogrammes et les règles de sécurité
Pour limiter les risques liés à l’utilisation de produits dangereux, il existe des pictogrammes pour indiquer qu’il y a un danger et des règles de sécurité pour expliquer comment limiter les risques.
Cliquer ici pour plus d’explications et pour faire un exercice interactif.
les mélanges
Activité 1 : corps pur ou mélange ?
Un mélange contient plusieurs espèces chimiques (plusieurs substances).
Beaucoup de substances dans la nature sont des mélanges : l’air, l’eau des rivières et des océans, le sang, le jus d’orange…
Un corps pur n’est composé que d’une espèce chimique (une seule substance)
Il existe des corps pur dans la nature comme l’or (pépite d’or), le dioxygène et le diazote (les deux gaz qui composent majoritairement l’air).
L’eau pure est rare dans la nature car beaucoup de substances peuvent se dissoudre dedans. Sous forme de vapeur d’eau, l’eau est pure.
activité 2 : mélange homogène ou mélange hétérogène ?
On peut mélanger certaines substances sans créer de nouveaux produits : on dit qu’il y a transformation physique.
Par exemple, si on mélange de l’eau et du sucre, le sucre se dissout dans l’eau : il est toujours présent dans l’eau même si on ne le voit plus.
Il existe deux types de mélanges : les mélanges homogènes et les mélanges hétérogènes. Cliquer ici pour en savoir plus et avoir accès aux exercices interactifs.
activité 3 : réaliser des mélanges et choisir le bon vocabulaire pour le décrire.
Pour savoir si un solide est soluble dans un liquide, il faut réaliser un test de solubilité.
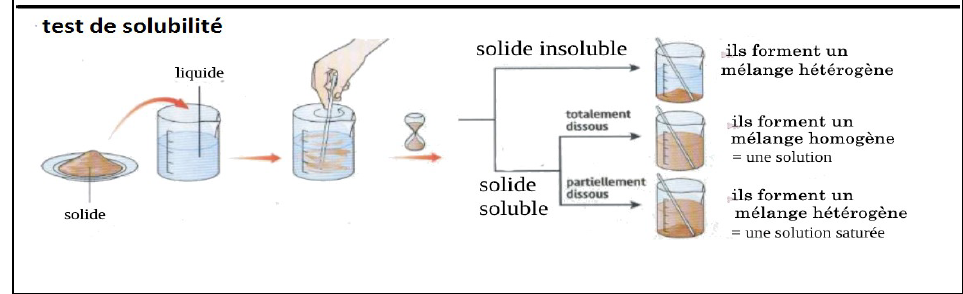
Pour savoir si un liquide est miscible avec un autre liquide, il faut réaliser un test de miscibilité.
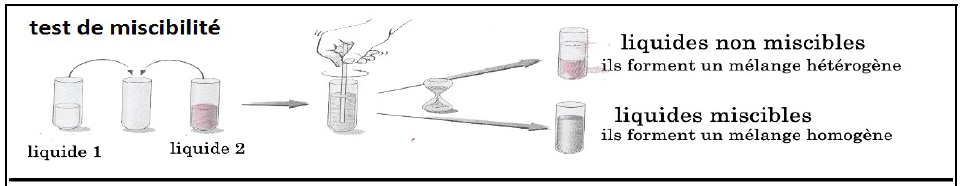
les techniques de séparation
Activité 1 : récupérer le sel comme dans la baie du Mont Saint Michel
Autrefois, les sauniers de la baie du Mont Saint Michel récupéraient le sel qui était mélangé au sable sur les grèves. Clique ici pour revoir l’activité réalisée en classe, avec les explications.
activité 2 : les techniques de séparation pour les mélanges hétérogènes
Pour les mélanges solides-liquides hétérogène, on utilise :
– la décantation : La décantation consiste à laisser reposer le mélange pour que les particules les plus denses se déposent au fond du récipient.
On obtient un mélange hétérogène dont les constituants se trouvent dans des parties différentes que l’on peut séparer plus facilement par la suite.
On réalise souvent une décantation avant de réaliser une filtration car cela empêche que le filtre soit bouché trop facilement par des particules les plus grosses.
– la filtration : La filtration consiste à faire passer le mélange à travers un filtre. Un filtre contient des trous plus ou moins gros : le filtre retient le solide insoluble et laisse passer la partie liquide du mélange. La grosseur des trous du filtre détermine la taille des particules qui sont retenues par la filtre.
cliquer ici pour voir des vidéos montrant une décantation et une filtration et un exercice interactif.
Exemple d’objets au quotidien qui utilise la technique de la filtration : la cafetière à filtre, la passoire, l’essoreuse à salade…
Un exemple pratique d’utilisation des techniques de séparation : le traitement des eaux usées.
Pour les mélanges liquides-liquides hétérogène, on utilise :
– la décantation liquide-liquides : La décantation liquide-liquide permet de séparer des liquides non-miscibles de densité différentes.
On laisse reposer le mélange. Il va se séparer en plusieurs phases : le liquide le plus dense se retrouve au fond tandis que le liquide le moins dense se retrouve au dessus.
En utilisant une ampoule à décanter, on peut récupérer les liquides l’un après l’autre dans des récipients différents.
activité 3 : les techniques de séparation pour les mélanges homogènes
La technique utilisée dépend du type de mélange.
Pour les mélanges solides-liquides homogène, on utilise :
– l’évaporation : en chauffant, le liquide s’évapore et le solide dissous va se cristalliser, c’est-à-dire qu’il va se déposer sous forme de solide dans le récipient. Le solide que l’on obtient après évaporation est appelé “résidu sec”.
Pour les mélanges liquides-liquides homogène, on utilise :
– la distillation : chaque corps pur liquide va bouillir à une température particulière. En chauffant un mélange contenant plusieurs liquides miscibles, les liquides vont s’évaporer l’un après l’autre.
Exemple d’utilisation de la distillation au quotidien :
vidéo : le raffinage du pétrole
vidéo La fabrication de la fleur d’oranger
– la chromatographie : cette technique permet surtout de déterminer si une substance est un corps pur ou un mélange; elle peut servir à identifier les différents constituants d’un mélange homogène. Un liquide (solvant) va monter le long d’une plaque ou d’une feuille par capillarité en entraînant plus ou moins bien les constituants du mélange : ceux -ci vont monter à des hauteurs différentes et vont pouvoir être séparés ainsi.
Exercices interactifs
Deux exercices interactifs pour s’entrainer sur les techniques de séparation.
Plusieurs exercices pour s’entraîner avec le vocabulaire des mélanges
masse et volume
Activité 1 : mesure de masse
La masse permet de mesurer la quantité de matière dans un objet.
Elle se mesure avec une balance.
Elle s’exprime en kilogramme (kg) ou en gramme (g)
On utilise la lettre « m » pour écrire une mesure : mobjet = 205 g
Comment mesurer une masse : une animation pour revoir la méthode à suivre.
Attention ! Dans la vie courante, on dit le mot « poids » à la place du mot « masse« .
En Sciences, le poids d’un objet correspond à la force avec laquelle la Terre nous attire vers elle : il explique pourquoi un objet tombe et s’exprime en newton (N).
IL NE FAUT PAS UTILISER LE MOT « poids » QUAND ON UTILISE UNE BALANCE OU QUAND ON MESURE EN KILOGRAMME : IL FAUT UTILISER LE MOT « MASSE« .
activité 2 : mesure de volume
Le volume permet de mesurer l’espace qu’occupe l’objet.
Il se mesure avec un récipient gradué, comme l’éprouvette.
Un récipient comme le bécher permet de mesurer un volume mais pas de manière précise. On utilisera donc une éprouvette.
Il s’exprime en mètre cube (m3) ou en litre (L)
On utilise la lettre « V » pour écrire une mesure : Vobjet = 150 mL
Des exercices interactifs pour s’entraîner à mesurer une masse et des volumes.
activité 3 : les unités et les conversions
La plupart des unités sont découpées en multiples et en sous-multiples, ce qui permet d’avoir des nombres ni trop petits, ni trop grand.
Pour toutes les unités que nous voyons au collège (sauf pour les unités du temps), on se sert du même tableau de multiples et de sous-multiples, et en particulier les colonnes en vert et en orange.
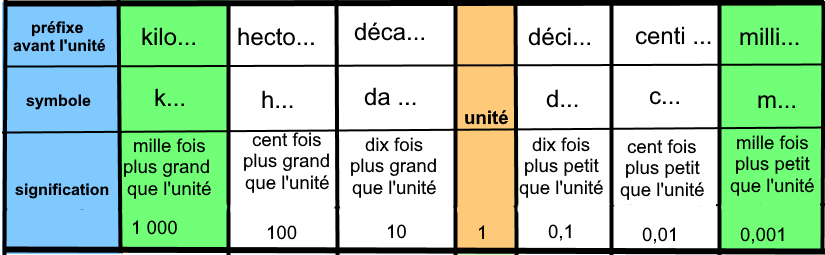
Les conversions : unité, multiple et sous-multiples – exercice interactif pour bien comprendre le principe.
le système solaire (et l’univers)
Les phases de la Lune




