Activité 1 : De quoi est constituée la matière autour de nous ?
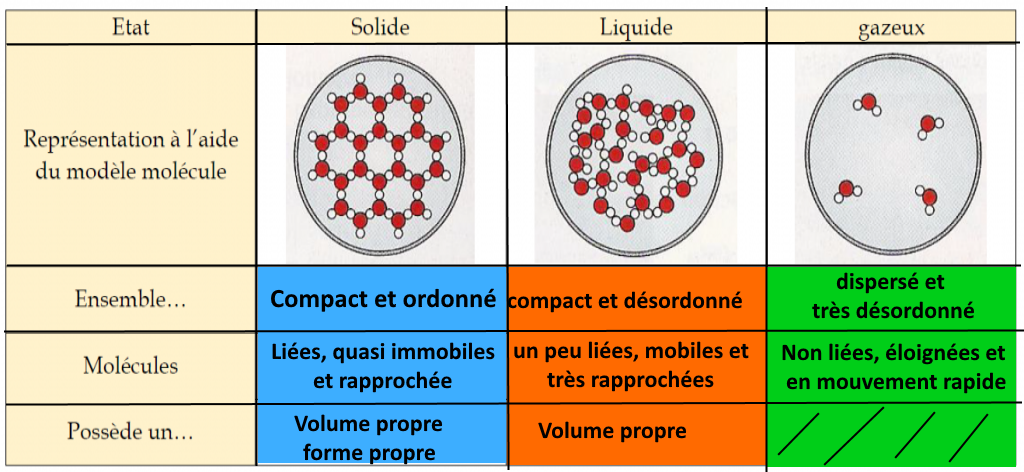
les 3 états au niveau microscopique (ou niveau moléculaire)
En cliquant ICI, tu pourras observer les 3 états de l’eau au niveau microscopique, c’est-à-dire au niveau des molécules.
deux vidéos qui permet de “voir” les molécules à l’intérieur de l’eau dans l’état liquide, solide et gazeux
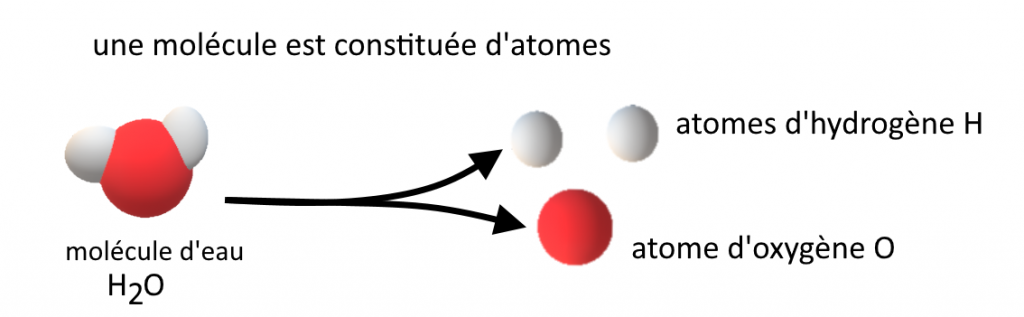
La matière est constituée d’atomes, qui peuvent se regroupés en molécules.
Atomes et molécules sont des particules invisibles même avec un microscope optique. Les molécules qui constituent un corps pur sont toutes identiques (même forme, même volume, même masse). Elles sont séparées par du vide.
La molécule est le plus petit “morceau” d’une espèce chimique : toutes les molécules d’une espèce chimiques sont identiques (même forme, même taille, même masse)

La disposition des molécules change selon l’état de la matière mais les molécules restent les mêmes.
plusieurs exercices pour s’entraîner sur les modèles
La différence entre un corps pur et un mélange au niveau moléculaire.
Chaque espèce chimique est représentée par une molécule donc :
– Un corps pur n’est composé que d’une seul type de molécules.
– Un mélange contient plusieurs types de molécules (un type par espèce chimique)

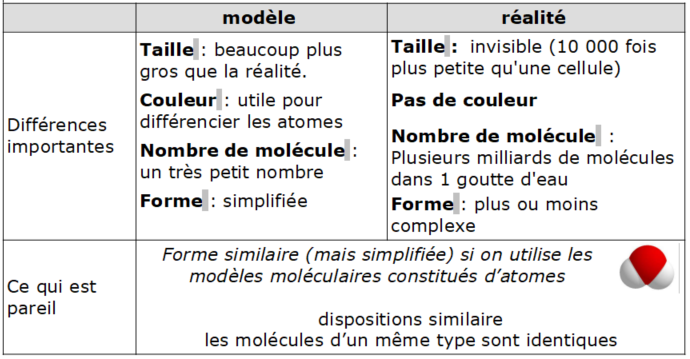
Pourquoi utiliser un modèle ?
Un modèle permet de représenter la réalité, de façon plus ou moins correctement, afin d’expliquer et de mieux comprendre certains phénomènes → pour simplifier, les molécules peuvent être modélisées par des formes géométriques.
Différence entre le modèle et la réalité