à l’échelle macroscopique
La matière existe principalement sous trois états : l’état solide, l’état liquide et l’état de gaz.
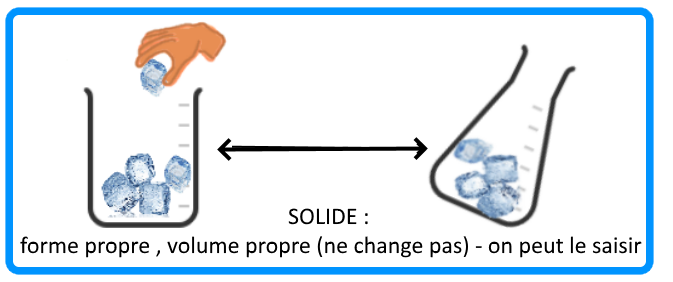
Un solide a une forme propre et un volume propre (= son volume et sa forme ne changent pas). On peut saisir un solide et il est incompressible (= son volume ne peut pas diminuer).
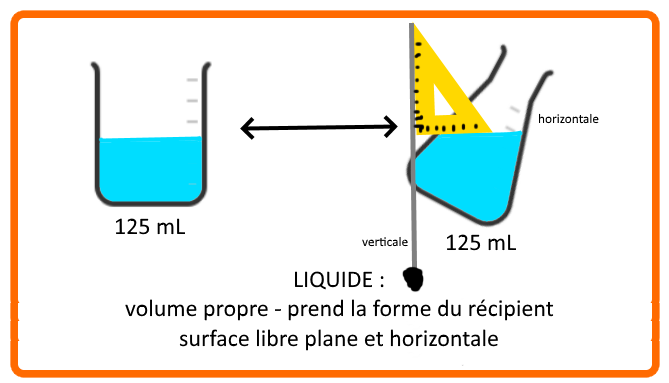
un liquide a un volume propre mais il prend la forme du récipient qui le contient. Il est incompressible. Sa surface libre est plane et horizontale.
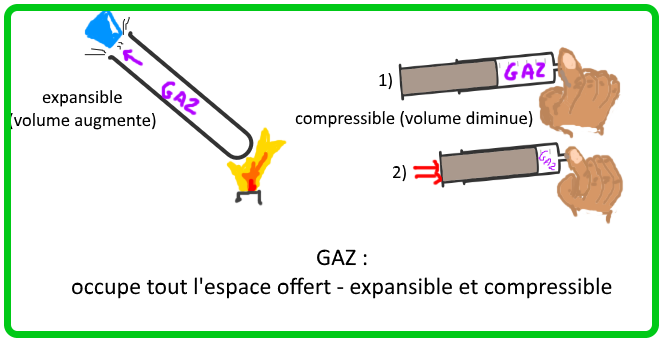
Un gaz n’a pas de volume ni de forme propre : il occupe tout l’espace offert. Un gaz est expansible (= son volume peut augmenter) et compressible (= son volume peut diminuer)
Pages : 1 2




