Activité 3 : changements d’états
Pour commencer, une animation de la cité des sciences pour expliquer la différence entre température et chaleur.
A) Les noms des changements d’état.
Un changement d’état est le passage d’un état à un autre.
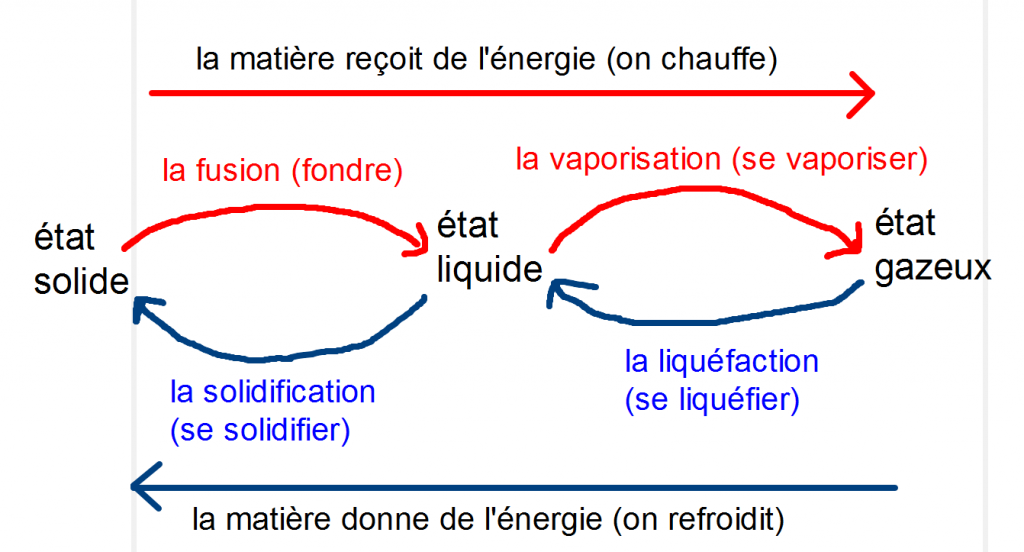
Remarque : Lorsqu’on chauffe une matière, les molécules sont de plus en plus mobiles.
B) les températures des changements d’état.
Lors d’un changement d’état d’un corps pur, on observe un palier de température sur la courbe des variations de la température en fonction du temps : la température reste la même pendant toute la durée du changement d’état.
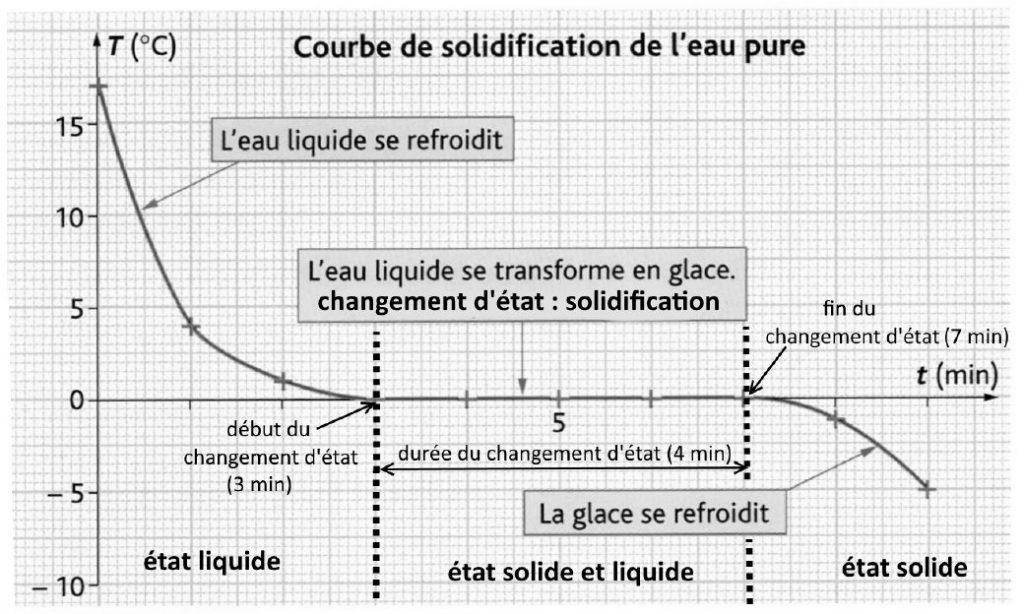
Les températures de changement d’état sont caractéristiques d’un corps pur. Par exemple, l’eau pure se solidifie/la glace fond à 0°C et l’eau pure bout à 100°C, à pression normale.
(voir quelques températures de fusion et d’ébullition sur wikipédia)
Les températures de changement d’état dépendent de la pression : par exemple, la température d’ébullition de l’eau augment si la pression augmente (principe de l’autocuiseur).
MELANGE : pendant le changement d’état d’un mélange, la température varie. On n’observe pas de palier de température.
C) Masse et volume lors des changements d’état.
Lors d’un changement d’état, la masse ne change pas (il y a toujours autant de molécules) mais le volume peut changer (les molécules se disposent autrement)
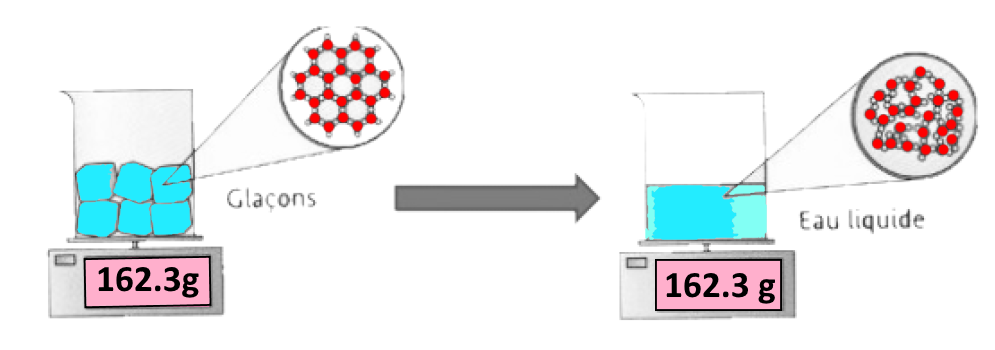
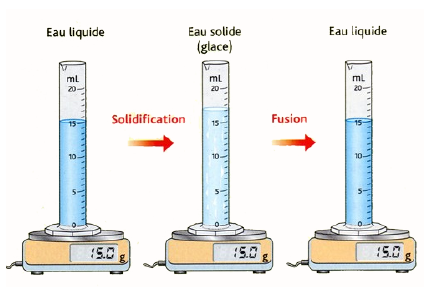
La masse vaut toujours 15,0 grammes
Le volume de la glace vaut 17 mL alors que le volume de l’eau correspondant vaut 15 mL.




